Mới đây, Cục Quản lý Dược (Bộ Y tế) đã ban hành văn bản số 1997//QLD-MP yêu cầu đình chỉ lưu hành, thu hồi và tiêu hủy mỹ phẩm không đạt tiêu chuẩn chất lượng.
Lô mỹ phẩm bị đình chỉ, thu hồi là Sữa chống nắng DSK UV, hộp 1 tuýp 35g, số tiếp nhận phiếu công bố 16682/23/CBMP-HN, số lô 2308008; NSX 19/08/2023, HSD 18/08/2026.
Lý do thu hồi, do mẫu kiểm nghiệm không đạt tiêu chuẩn chất lượng về chỉ tiêu giới hạn vi sinh vật.
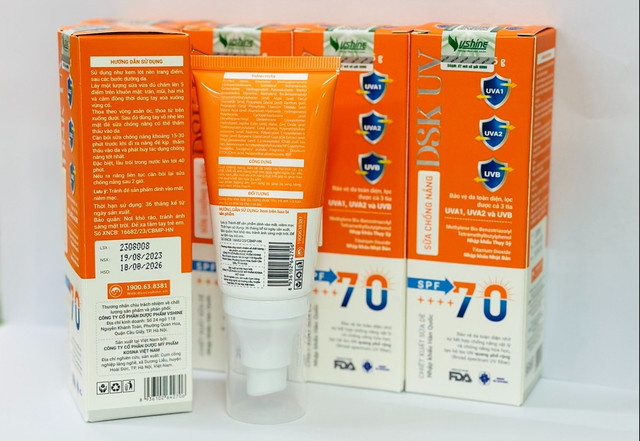

Sản phẩm do Công ty Cổ phần Dược mỹ phẩm Kosna Việt Nam sản xuất tại cụm công nghiệp làng nghề, xã Dương Liễu, TP Hà Nội. Công ty Cổ phần Dược phẩm Vshine (địa chỉ kinh doanh tại số 24 ngõ 118 Nguyễn Khánh Toàn, phường Quan Hoa, quận Cầu Giấy (cũ), TP Hà Nội) chịu trách nhiệm đưa sản phẩm ra thị trường.
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố trực thuộc Trung ương thông báo đến các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng lô sản phẩm bị thu hồi và yêu cầu trả lại cơ sở cung ứng. Các đơn vị liên quan cần tổ chức thu hồi, tiêu hủy lô sản phẩm vi phạm, đồng thời kiểm tra, giám sát việc thực hiện thông báo và xử lý vi phạm theo quy định.
Công ty Cổ phần Dược phẩm VShine và Công ty Cổ phần Dược mỹ phẩm Kosna Việt Nam có trách nhiệm gửi thông báo thu hồi đến tất cả các điểm phân phối, sử dụng lô sản phẩm; Tiếp nhận hàng hóa trả lại, thực hiện tiêu hủy toàn bộ lô sản phẩm không đạt chất lượng; Gửi báo cáo về Cục Quản lý Dược trước ngày 11/8/2025.
Sở Y tế TP Hà Nội được giao nhiệm vụ giám sát hai công ty trên trong quá trình thực hiện việc thu hồi, tiêu hủy, đồng thời kiểm tra việc chấp hành quy định pháp luật về sản xuất, kinh doanh mỹ phẩm. Cơ quan này cũng được yêu cầu xác minh tính chính xác của địa chỉ tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường ghi trên nhãn so với hồ sơ công bố và xử lý vi phạm nếu có. Kết quả kiểm tra, giám sát phải được báo cáo về Cục Quản lý Dược trước ngày 26/8/2025.