Ngày 08/10/2025, Cục Quản lý Dược (Bộ Y tế) vừa ban hành Quyết định số 532/QĐ-QLD về việc thu hồi 8 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm của Công ty TNHH đầu tư thương mại XNK ASEAN (địa chỉ: Số 10, ngách 91, ngõ 634, đường Kim Giang, xã Thanh Liệt, huyện Thanh Trì (cũ), thành phố Hà Nội).
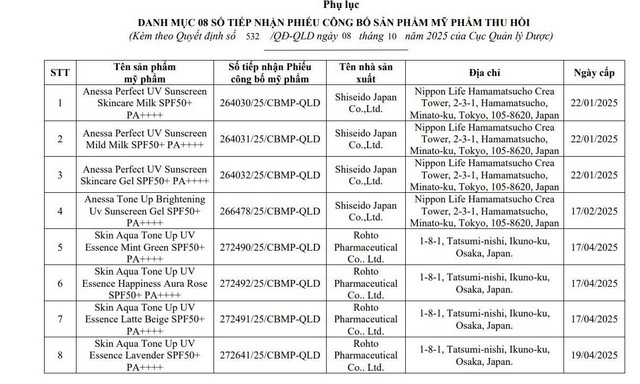
Cụ thể, thu hồi 8 số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm do Cục Quản lý Dược cấp đối với các sản phẩm mỹ phẩm:
Anessa Perfect UV Sunscreen Skincare Milk SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 264030/25/CBMP-QLD;
Anessa Perfect UV Sunscreen Mild Milk SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 264031/25/CBMP-QLD;
Anessa Perfect UV Sunscreen Skincare Gel SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 264032/25/CBMP-QLD;
Anessa Tone Up Brightening Uv Sunscreen Gel SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 266478/25/CBMP-QLD;
Skin Aqua Tone Up UV Essence Mint Green SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 272490/25/CBMP-QLD;
Skin Aqua Tone Up UV Essence Happiness Aura Rose SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 272492/25/CBMP-QLD;
Skin Aqua Tone Up UV Essence Latte Beige SPF50+ PA++++, Số tiếp nhận Phiếu công bố mỹ phẩm 272491/25/CBMP-QLD;
Skin Aqua Tone Up UV Essence Lavender SPF50+ PA++++, 272641/25/CBMP-QLD.
Các sản phẩm trên do Shiseido Japan Co.,Ltd và Rohto Pharmaceutical Co.. Ltd. sản xuất.
Các sản phẩm do Công ty TNHH đầu tư thương mại XNK ASEAN (địa chỉ: Số 10, ngách 91, ngõ 634, đường Kim Giang, xã Thanh Liệt, huyện Thanh Trì, TP Hà Nội) chịu trách nhiệm đưa sản phẩm ra thị trường.
Lý do thu hồi do công ty đề nghị thu hồi tự nguyện số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm vì không có nhu cầu kinh doanh. Công ty cam kết chưa nhập khẩu, phân phối và lưu hành 8 sản phẩm nêu trên tại thị trường Việt Nam.
Quyết định này có hiệu lực kể từ ngày ký ban hành và thay thế Quyết định số 529/QĐ-QLD ngày 07/10/2025 của Cục Quản lý Dược về việc thu hồi số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm, do Quyết định số 529/QĐ-QLD ngày 07/10/2025 ban hành thiếu mục nơi nhận.
Giám đốc Công ty TNHH đầu tư thương mại XNK ASEAN và Giám đốc Sở Y tế các tỉnh, thành phố trực thuộc Trung ương chịu trách nhiệm thi hành Quyết định.
Số tiếp nhận phiếu công bố do cơ quan nhà nước cấp khi doanh nghiệp đăng ký sản phẩm. Số này xác nhận sản phẩm đã được tổ chức, cá nhân chịu trách nhiệm công bố trước khi lưu hành trên thị trường. Thời hạn hiệu lực của số tiếp nhận là 5 năm kể từ ngày cấp. Nhà chức trách sẽ thu hồi số này nếu tổ chức hoặc cá nhân có văn bản đề nghị hoặc khi sản phẩm vi phạm quy định.
















