Cục Quản lý dược (Bộ Y tế) vừa có thông báo đình chỉ lưu hành, thu hồi trên toàn quốc lô sản phẩm Hanayuki Sunscreen Body - hộp 1 tuýp 100 gram. Đây là sản phẩm kem chống nắng cho da.
Sản phẩm Hanayuki Sunscreen Body - hộp 1 tuýp 100 gram bị yêu cầu thu hồi
Trên nhãn ghi số tiếp nhận PCB: 779/24/CBMP-ĐN; số lô: 0010125; NSX: 060125; HD: 050127. Sản phẩm này do Công ty TNHH thương mại dịch vụ VB Group (địa chỉ: tầng lửng cao ốc Đại Thanh Bình, số 911-913-915-917 Nguyễn Trãi, phường 14, quận 5, TP HCM) tổ chức chịu trách nhiệm đưa sản phẩm ra thị trường. Công ty TNHH EBC Group (địa chỉ đường số 6, KCN Giang Điền, xã Giang Điền, huyện Trảng Bom, tỉnh Đồng Nai) sản xuất.
Kết quả kiểm nghiệm do Viện Kiểm nghiệm thuốc TP HCM thực hiện cho thấy chỉ số chống nắng trên nhãn (SPF 50) không phù hợp với kết quả kiểm nghiệm chỉ số chống nắng của mẫu thử (SPF là 2,4).
Theo phiếu công bố sản phẩm do Sở Y tế tỉnh Đồng Nai cấp cho sản phẩm mỹ phẩm Hanayuki Sunscreen Body, sản phẩm công dụng "bảo vệ da chống nắng, dưỡng da và làm trắng da toàn thân", không ghi thông tin có chỉ số chống nắng SPF là 50 như trên nhãn sản phẩm lưu thông.
Chuyên gia cho biết SPF là chỉ số đo khả năng chống tia UVB- loại tia gây hại cho da.

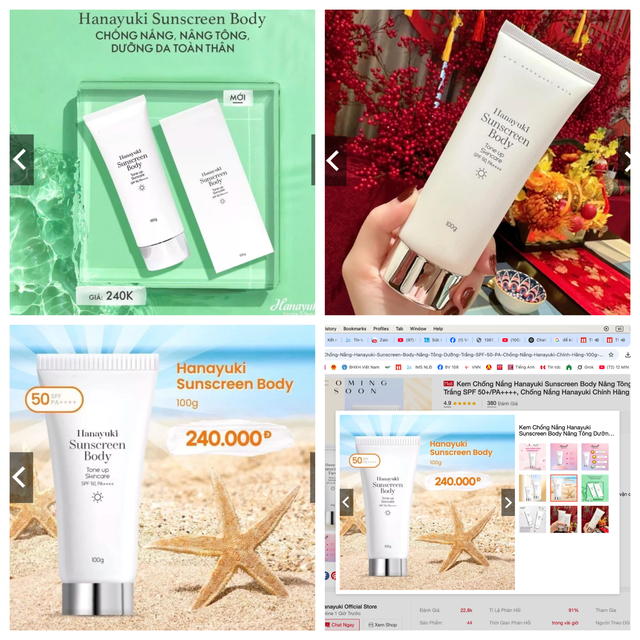
Sản phẩm được quảng cáo trên sàn thương mại điện tử. Ảnh chụp màn hình
Vì thế, Cục Quản lý dược đề nghị ngừng ngay việc kinh doanh, sử dụng lô sản phẩm trên và trả lại cơ sở cung ứng sản phẩm. Các địa phương tiến hành thu hồi lô sản phẩm vi phạm nêu trên; kiểm tra, giám sát các đơn vị thực hiện thông báo này; xử lý các đơn vị vi phạm theo quy định hiện hành.
Công ty TNHH thương mại dịch vụ VB Group, Công ty cổ phần nhà máy y tế EBC Đồng Nai phải gửi thông báo thu hồi tới những nơi phân phối, sử dụng lô sản phẩm nêu trên. Đồng thời tiếp nhận sản phẩm trả lại từ các cơ sở kinh doanh và tiến hành thu hồi toàn bộ sản phẩm không đáp ứng quy định.
Trường hợp không loại bỏ yếu tố vi phạm (không thể tách rời nhãn hàng hóa vi phạm ra khỏi hàng hóa) thì buộc tiêu hủy sản phẩm theo quy định.
































