Ngày 27/8/2025, Cục Quản lý Dược (Bộ Y tế) đã ban hành Công văn số 2488/QLD-MP về việc đình chỉ lưu hành, thu hồi mỹ phẩm vi phạm về ghi nhãn của Công ty Cổ phần Thương mại Dược phẩm Quang Minh.
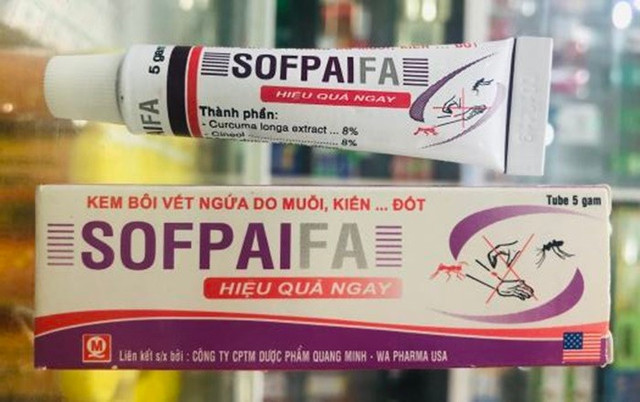
Theo đó, Cục Quản lý Dược thông báo đình chỉ lưu hành, thu hồi trên toàn quốc lô sản phẩm Sofpaifa – Hộp 1 tuýp 5g. Trên nhãn ghi số tiếp nhận PCB 002220/20/CBMP-HCM, số lô 0010724, NSX 160724, HD 160727. Sản phẩm do Công ty Cổ phần Thương mại Dược phẩm Quang Minh (địa chỉ: Số 4A Lò Lu, phường Trường Thạnh, thành phố Thủ Đức, TP HCM, nay là số 4A Lò Lu, phường Long Phước, TP HCM) sản xuất và chịu trách nhiệm đưa sản phẩm ra thị trường.

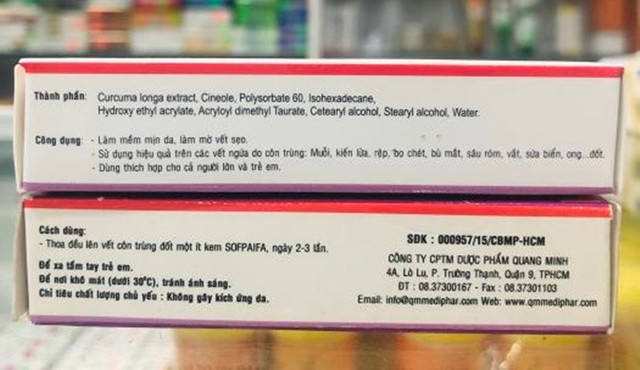
Lý do thu hồi là nhãn, hướng dẫn sử dụng chứa các cụm từ, hình ảnh không phù hợp tính năng, công dụng của sản phẩm mỹ phẩm và thông tin trên Phiếu công bố. Cụ thể sử dụng các cụm từ “Kem bôi vết ngứa do muỗi, kiến… đốt”, “Sử dụng hiệu quả trên các vết ngứa do côn trùng: muỗi, kiến lửa, rệp, bọ chét, bù mắt, sâu róm, vắt, sứa biển, ong… đốt”, “có tính chống ngứa, sát trùng, làm êm dịu da”.
Mẫu mỹ phẩm trên do Trung tâm kiểm nghiệm thuốc, mỹ phẩm, thực phẩm – Sở Y tế TP Hà Nội lấy mẫu tại Công ty Cổ phần Thương mại Dược phẩm Nam An (địa chỉ: Quầy 342, tầng 3 Trung tâm phân phối dược phẩm và trang thiết bị y tế Hapu, tòa nhà 24 T1, số 1 Nguyễn Huy Tưởng, Thanh Xuân, TP Hà Nội) để kiểm tra.
Cục Quản lý Dược đề nghị Sở Y tế các tỉnh, thành phố thông báo cho các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn ngừng ngay việc kinh doanh, sử dụng lô sản phẩm Sofpaifa - Hộp 1 tuýp 5g nêu trên và trả lại cơ sở cung ứng sản phẩm; Tiến hành thu hồi lô sản phẩm vi phạm; Kiểm tra, giám sát các đơn vị thực hiện thông báo này; Xử lý các đơn vị vi phạm theo quy định hiện hành.
Công ty Cổ phần Thương mại Dược phẩm Quang Minh phải gửi thông báo thu hồi tới những nơi phân phối, sử dụng lô sản phẩm Sofpaifa - Hộp 1 tuýp 5g nêu trên; Tiếp nhận sản phẩm trả lại từ các cơ sở kinh doanh và tiến hành thu hồi lô sản phẩm không đáp ứng quy định. Trường hợp không loại bỏ yếu tố vi phạm (không thể tách rời nhãn hàng hóa vi phạm ra khỏi hàng hóa) thì buộc tiêu hủy lô sản phẩm; Gửi báo cáo thu hồi lô sản phẩm về Cục Quản lý Dược trước ngày 22/9/2025.
Rà soát nội dung ghi trên nhãn, hướng dẫn sử dụng đối với các lô khác đã sản xuất của sản phẩm vi phạm, trường hợp có lỗi tương tự như lô sản phẩm vi phạm nêu trên, công ty phải khẩn trương thông báo thu hồi đến các cơ sở phân phối, sử dụng và gửi báo cáo việc rà soát, thu hồi sản phẩm về Cục Quản lý Dược trước ngày 07/9/2025. Công ty chịu hoàn toàn trách nhiệm trước pháp luật nếu báo cáo không trung thực.
Bên cạnh đó, Cục Quản lý Dược đề nghị Sở Y tế TP HCM giám sát Công ty Cổ phần Thương mại Dược phẩm Quang Minh trong việc thực hiện thu hồi lô sản phẩm Sofpaifa - Hộp 1 tuýp 5g không đáp ứng quy định; Kiểm tra công ty trong việc chấp hành các quy định của pháp luật về quản lý mỹ phẩm trong hoạt động sản xuất, kinh doanh mỹ phẩm; Xử lý, xử phạt vi phạm theo quy định hiện hành. Báo cáo kết quả kiểm tra, giám sát về Cục Quản lý Dược trước ngày 07/10/2025.