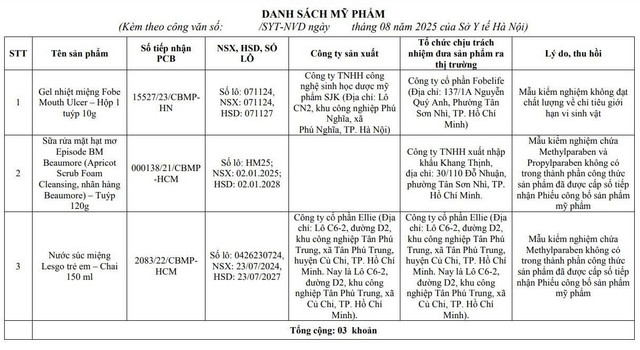
Sở Y tế Hà Nội đã có thông báo số 4456/SYT-NVD ngày 25/8/2025 về việc đình chỉ lưu hành, yêu cầu thu hồi 3 lô mỹ phẩm vi phạm trên địa bàn thành phố. Cụ thể các sản phẩm vi phạm gồm:
Sản phẩm Gel nhiệt miệng Fobe Mouth Ulcer – hộp 1 tuýp 10g; Số tiếp nhận phiếu công bố 15527/23/CBMPHN; Số lô 071124, NSX 071124, HSD 071127; Sản phẩm do Công ty TNHH công nghệ sinh học dược mỹ phẩm SJK (địa chỉ: Lô CN2, khu công nghiệp Phú Nghĩa, xã Phú Nghĩa, TP Hà Nội) sản xuất; Công ty Cổ phần Fobelife (Địa chỉ: 137/1A Nguyễn Quý Anh, Phường Tân Sơn Nhì, TP HCM) chịu trách nhiệm đưa sản phẩm ra thị trường. Lý do thu hồi do mẫu kiểm nghiệm không đạt chất lượng về chỉ tiêu giới hạn vi sinh vật.

Ảnh minh hoạ/Nguồn sohuutritue.net
Sản phẩm Sữa rửa mặt hạt mơ Episode BM Beaumore (Apricot Scrub Foam Cleansing, nhãn hàng Beaumore) – Tuýp 120g; Số tiếp nhận phiếu công bố 000138/21/CBMP-HCM; Số lô HM25, NSX 02.01.2025, HSD 02.01.2028. Công ty TNHH xuất nhập khẩu Khang Thịnh (địa chỉ: 30/110 Đỗ Nhuận, phường Tân Sơn Nhì, TP HCM) chịu trách nhiệm đưa sản phẩm ra thị trường. Lý do thu hồi là mẫu kiểm nghiệm chứa Methylparaben và Propylparaben không có trong thành phần công thức sản phẩm đã được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
Sản phẩm Nước súc miệng Lesgo trẻ em – Chai 150 ml; Số tiếp nhận phiếu công bố 2083/22/CBMPHCM; Số lô 0426230724, NSX 23/07/2024, HSD 23/07/2027. Công ty Cổ phần Ellie (địa chỉ: Lô C6-2, đường D2, khu công nghiệp Tân Phú Trung, xã Tân Phú Trung, huyện Củ Chi, TP HCM, nay là Lô C6-2, đường D2, khu công nghiệp Tân Phú Trung, xã Củ Chi, TP HCM) sản xuất và chịu trách nhiệm đưa sản phẩm ra thị trường. Lý do thu hồi do mẫu kiểm nghiệm chứa Methylparaben không có trong thành phần công thức sản phẩm đã được cấp số tiếp nhận Phiếu công bố sản phẩm mỹ phẩm.
Sở Y tế Hà Nội đề nghị UBND xã, phường thông báo cho các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn tiến hành thu hồi toàn bộ lô sản phẩm nêu trên; Kiểm tra, giám sát việc thực hiện thu hồi của các cơ sở (nếu có).
Các cơ sở kinh doanh, sử dụng mỹ phẩm trên địa bàn khẩn trương rà soát, ngừng ngay việc kinh doanh, sử dụng các lô sản phẩm nêu trên và trả lại cơ sở cung ứng sản phẩm;
Văn phòng - Sở Y tế Hà Nội đăng thông tin, phối hợp với các cơ quan truyền thông thông tin tới các cơ sở kinh doanh, sử dụng mỹ phẩm và người dân biết để không buôn bán, sử dụng. Sở Y tế thông báo để các cơ sở, đơn vị biết, thực hiện và báo cáo việc thực hiện về Sở Y tế.